istoiredesNeurosciences
LA LETTRE
N°53
nue lenombredesvésiculescontenantdescatécholamines
— l’adrénalineet lanoradrénaline—dans les terminaisons
nerveusesdusystèmepériphérique.Carlssonsupposeque,
dans lesystèmenerveuxcentral, la réserpine«vide»aussi
le stock de catécholamines, cequi expliquerait ses effets
neuroleptiquesà forteconcentration.
Comment prouver cette hypothèse? En reconstituant le
stockdescatécholaminesdans les terminaisonsnerveuses,
Carlsson espère empêcher la réserpined’agir. Mais il ren-
contredeux obstacles. D’unepart, les catécholamines ne
traversent pas labarrièrehématoencéphalique, qui isole le
cerveaudu restede l’organisme.D’autrepart, les techniques
disponiblesnepermettent pasdemesurer lesquantitésde
catécholaminesdans lecerveau.
Carlsson lèvecesdeuxobstaclesen impliquantdeuxsubs-
tances connues, la L-dopa et la dopamine. Le chimiste
GeorgeBarger a synthétisé la dopamine en 1910. Quant
à laL-dopa, elleest identifiéedans les tissus animauxdès
1913par lebiochimisteMarkusGuggenheim. Par ailleurs,
depuis1937, grâceaux travauxdeHermannBlashkoet de
PeterHoltz, onconnaît la séquencemétaboliquedescaté-
cholamines,c’est-à-dire l’ensembledes réactionschimiques
qui aboutissent à leur synthèse (Figure1).
Ainsi, on supposeque le seul intérêt de la L-dopa et de la
dopamineestd’êtredesprécurseursdescatécholamines…
Mais dans les années 1950, on connaît la neurotransmis-
sionchimiquedans le systèmenerveuxpériphériqueet on
cherchedessubstancespouvant jouer le rôledeneurotrans-
metteursdans lecerveau.Comme lanoradrénalineestdétec-
téedans lesystèmenerveuxpériphérique, on tented’abord
d’isoler les catécholamines dans les tissus cérébraux.
En1954, laneuroscientifiqueAllemandeMartheVogtmontre
que lesconcentrationscérébralesdenoradrénalinesont très
faibles, cequi provoque une certainedésillusion. Puis, en
1958, Carlssondéveloppeuneméthodededosage spéci-
fiquede ladopamine : elle est présentedans le cerveau,
peutique de lamaladie de Parkinson attribuable àChar-
cot préconisait d’utiliser des extraits de belladone (une
planteherbacée), richeenmoléculesnomméesalcaloïdes.
Cesdernièresatténuentcertainssignesde lamaladieet sont
alors leprincipal remèdeantiparkinsonien.Eneffet,quelques
symptômes, telsque les tremblements et l’hypersalivation,
évoquent unehyperexcitationdusystèmecérébral choliner-
gique,c’est-à-direunexcèsde fonctionnementdesneurones
transmettant de l’acétylcholinepour communiquer. Or, les
alcaloïdes sont des inhibiteurs naturels de ces neurones,
des anticholinergiques. Àpartir de 1945, on commence à
synthétiser chimiquement des anticholinergiques : trihexy-
phénidyle (Artane®), orphénadrine (Disipal®),profénamine
(Parsidol®),etc.Dans lesannées1950, lesseuls traitements
disponibles de lamaladiedeParkinson sont ces anticholi-
nergiqueset lachirurgie lésionnelledu faisceaupyramidal
oudesganglionsde labase.
LamaladiedeParkinson, uneaffairedechimie
Lesannéescinquantevoient lapénétrationauniveaucérébral
de la théorie chimiquede la neurotransmission, jusque-là
cantonnéeauniveaupériphérique. Cetteémergencede la
neurochimie cérébrale, largement issue des progrès des
techniquesd’exploration, vase traduirepar l’entréeenscène
de ladopamine.Pourcomprendrececi, il est nécessairede
faireundétour par lapharmacologie
(3)
.
En1955, lemédecinet neurobiologisteArvidCarlsson, de
l’UniversitédeLundenSuède, le futur lauréatduprixNobel
dephysiologieoumédecinede2000,étudie lemoded’action
de la réserpine, unemolécule qui vient d’être isolée par
les chimistes et qui est alorsprescriteà faibledosecontre
la dépression. En revanche, à fortes doses, la réserpine
aggrave ladépressionet les troublespsychotiques (onparle
d’effetsneuroleptiques).
Avec son compatriote chimisteNils-ÅkeHillarp, Carlsson
montre,chez l’animal,que l’administrationde réserpinedimi-
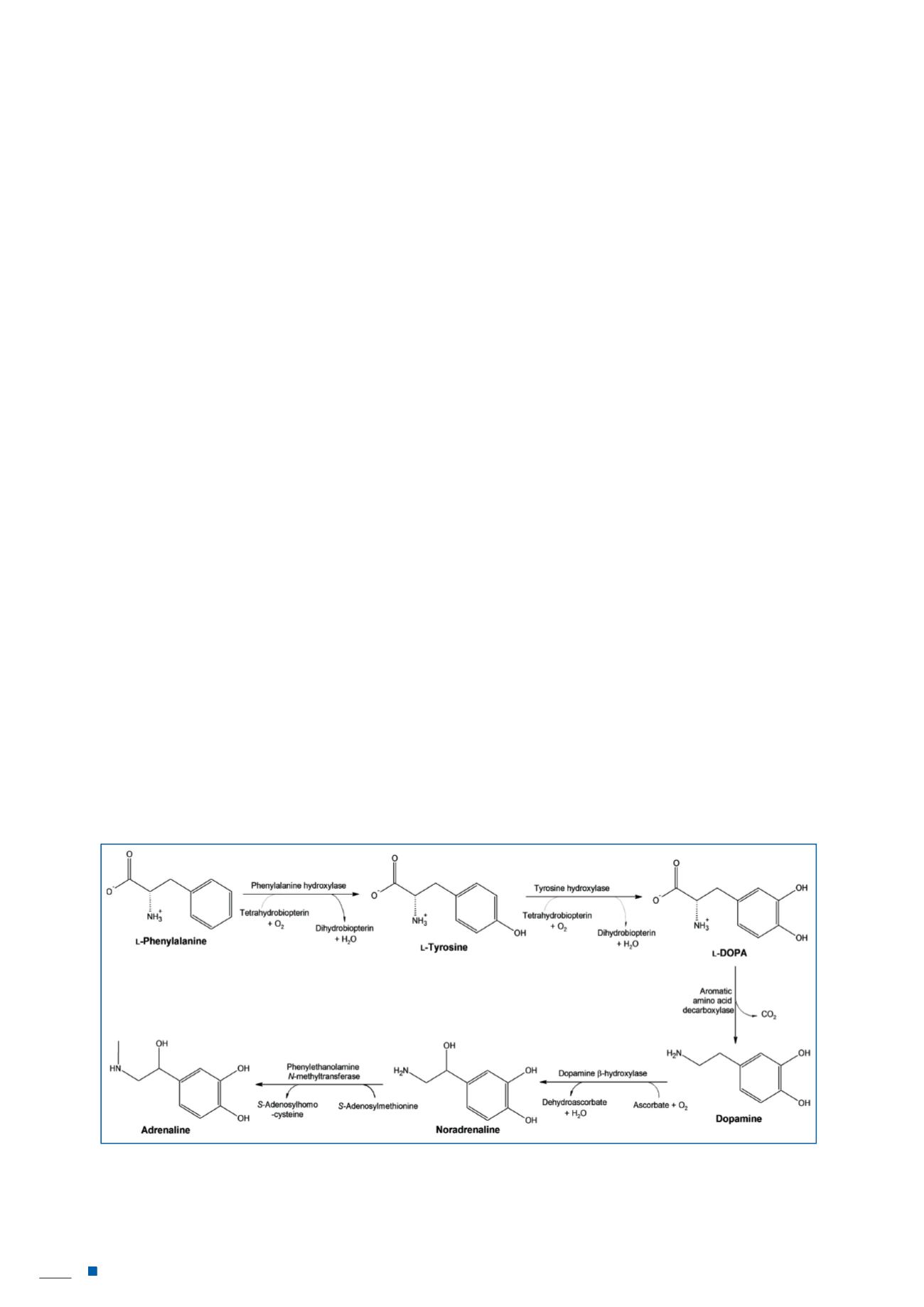
Figure1
-Métabolismedescatécholamines.Lesvoiesmétaboliquesde synthèsedescatécholaminespartentdedeuxacides
aminésessentiels laPhénylalanineet laTyrosine, la tyrosineétant leproduitde laphénylalaninehydroxylase.Une tyrosine
hydroxylaseoxydeànouveau lecyclearomatiquepourproduire ladihydroxyphénylalanine (DOPA).UneDOPAdécarboxylase
produit ladopamine, qui est ensuiteoxydéeennoradrénaline, puisméthyléeenadrénaline.


