Tag: Actualité
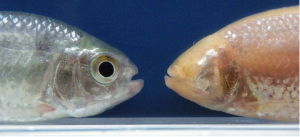
Un même poisson à quelques neurones hypocrétinergiques près
L’un est coloré et vit dans les rivières d’Amérique latine, l’autre est aveugle, dépigmenté et habite dans l’obscurité des grottes…

Lois de Bioéthique et Neurosciences
La Société des Neurosciences a été invitée à une audition dans le cadre des Etats généraux de la Bioéthique, organisés…
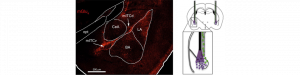
L’activation par la lumière de récepteurs endogènes dans l’amygdale soulage les symptômes associés à une douleur chronique inflammatoire
Devant la difficulté de traiter les douleurs chroniques, nous nous sommes interrogés sur les mécanismes centraux capables de moduler la…
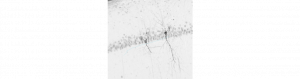
Tau et dégénérescences neurofibrillaires: toxiques OR NOT toxiques ?
Les tauopathies constituent un groupe de maladies neurodégénératives caractérisées par l’hyperphosphorylation de la protéine Tau et son accumulation sous forme…
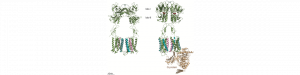
Contrôler l’activité des mGluR avec des nanobodies
Le neurotransmetteur de la grande majorité des synapses excitatrices, le glutamate, exerce aussi des rôles modulateurs via l’activation de récepteurs…
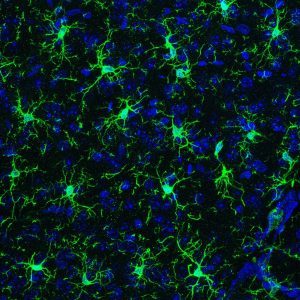
Microbiote et microglies: une inégalité des sexes !
Une étude conjointe entre des chercheurs Inserm de l’IBENS (Institut de Biologie de l’Ecole Normale Supérieure) à Paris et des…
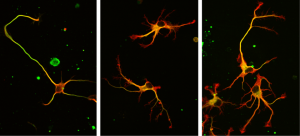
Une enzyme cruciale pour les neurones enfin démasquée !
L’équipe Physiopathologie du Cytosquelette de l’institut des Neurosciences de Grenoble a identifié l’enzyme responsable de la détyrosination de la tubuline…
Construire des ponts à travers les Neurosciences
Un article commun a dernièrement été publié dans Neuron, co-signé par des neuroscientifiques reconnus appartenant à un très large panel…
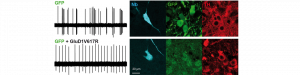
UN GÈNE ASSOCIÉ À LA SCHIZOPHRÉNIE CONTRÔLE L’ACTIVITÉ DES NEURONES DOPAMINERGIQUES
Une étude menée par Bertrand Lambolez et Ludovic Tricoire de l’unité Neuroscience Paris-Seine, parue le 11 juillet 2017 dans la…
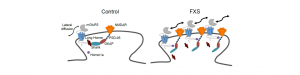
Les récepteurs synaptiques mGluR5 en mouvement : fauteurs de troubles dans le syndrome du X fragile
Le syndrome du X fragile (SXF) est la forme héréditaire la plus courante de déficience intellectuelle et une cause fréquente…
